Op 8 september 2021 kreeg ik een mailtje doorgestuurd van professor Kees Stam. De editor van het wetenschappelijk tijdschrift Network Neuroscience nodigde wetenschappers uit om een manuscript in te sturen voor publicatie, met de boodschap “The final deadline of October 1st for our Focus Feature on biomarkers is rapidly approaching!”. Over 23 dagen moest ons manuscript voor de pilot-studie dus worden ingediend bij de reviewers. Een klein probleem: er was nog geen manuscript.
MEG-netwerk-biomarker
Het is bekend dat functionele hersennetwerken verstoord worden door de ziekte van Alzheimer. Met behulp van magnetoencefalografie (MEG) kunnen afwijkingen in lokale hersenactiviteit en in de communicatie tussen hersengebieden worden gedetecteerd. Sensitieve biomarkers voor grootschalige ‘netwerk afwijkingen’ in de hersenen van Alzheimerpatiënten zijn echter schaars – zeker in een vroeg stadium van de ziekte. Wij hoopten daarom dat ons idee voor een mogelijke MEG-netwerk-biomarker succesvol zou zijn. Met een klein team onderzoekers gingen we de uitdaging aan om in drie weken tijd het concept uit te werken, analyses te doen en een compleet (en publiceerbaar) manuscript te produceren.
Informatieverwerking brein
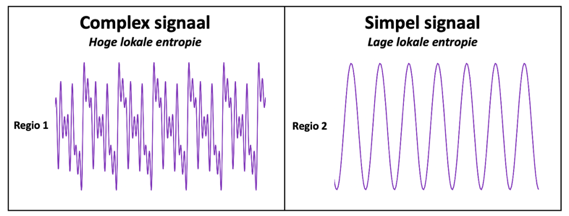
De nieuwe biomarker bouwt voort op een bestaand concept: entropie. Met behulp van entropie kunnen we de complexiteit van een hersensignaal kwantificeren. Simpele, voorspelbare signalen hebben lage entropie, waar complexe, variabele signalen hoge entropie hebben. Er bestaat een directe relatie tussen de variabiliteit en de informatie inhoud van een (hersen)signaal: een compleet voorspelbaar signaal bevat weinig tot geen informatie. Entropie kan ons dus mogelijk iets leren over (verstoorde) informatieverwerking in het brein. Voor onze studie vergeleken we de entropie van MEG signalen (afkomstig uit 80 individuele hersengebieden) van patiënten in een vroeg stadium van Alzheimer (Mild Cognitive Impairment, MCI) met patiënten met subjectieve geheugenklachten (Subjective Cognitive Decline, SCD). De lokale entropie was door het gehele brein significant hoger in MCI dan in SCD patiënten.
Communicatie tussen hersengebieden
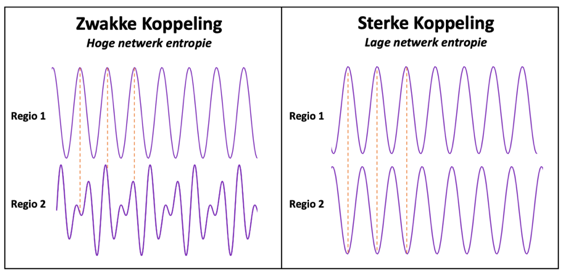
Na de lokale variabiliteit van hersensignalen te hebben vergeleken, berekenden we de entropie van het hersennetwerk. Hersengebieden communiceren met elkaar door hun activiteit op elkaar af te stemmen. Sterk verbonden gebieden laten vergelijkbare activatiepatronen zien. Netwerk entropie is in dat geval laag: er zit weinig variabiliteit in de koppeling tussen hersengebieden. Wanneer hersengebieden sterk verschillende activatiepatronen laten zien, is netwerk entropie hoog. De koppeling tussen regio’s is minder voorspelbaar en gebieden communiceren minder sterk met elkaar. De resultaten laten zien dat ook netwerk entropie significant hoger was in MCI dan SCD patiënten. De communicatie tussen hersengebieden lijkt dus te verzwakken, terwijl de complexiteit van hersenactiviteit op lokaal niveau juist toeneemt in MCI. In een laatste experiment werden SCD en MCI patiënten geclassificeerd op basis van netwerk entropie waarden. Met behulp van de nieuwe biomarker konden de patiëntgroepen succesvol worden onderscheden. Met de studie laten we zien dat netwerk entropie potentie heeft om al in een vroeg stadium van de ziekte van Alzheimer afwijkingen in functionele hersennetwerken te detecteren.
Succesvolle pilot-studie
Na flink wat uurtjes overleg, analyses, schrijven en herschrijven leverden we op 30 september het verslag van een succesvolle pilot-studie in. Op dit moment zijn we druk bezig om de biomarker technisch te verbeteren en om de fysiologische betekenis van veranderingen in (netwerk) entropie beter te begrijpen. Dat doen we ditmaal zonder bizarre deadline, maar mét hetzelfde enthousiasme, om zo hopelijk tot een nog beter resultaat te komen.
Meer weten?
De publicatie in Network Neuroscience is hier terug te lezen: Network-level permutation entropy of resting-state MEG recordings: a novel biomarker for early-stage Alzheimer’s disease? | Network Neuroscience | MIT Press.
Elliz Scheijbeler, promovenda Alzheimercentrum Amsterdam, Amsterdam UMC